従来のナノ医薬品(ナノメディシンとも呼ばれます)は、生体親和性の高い成分で構成されたリポソーム(生体膜と同じ構成成分であるリン脂質から構成されているナノカプセル)やアルブミンナノ粒子(アルブミンは生体内の血清タンパク)がほとんどでしたが、最近金属や無機材料が従来のものにはない性質を持っていることから臨床試験が行われています(Tagami & Ozeki JPS 2017)。
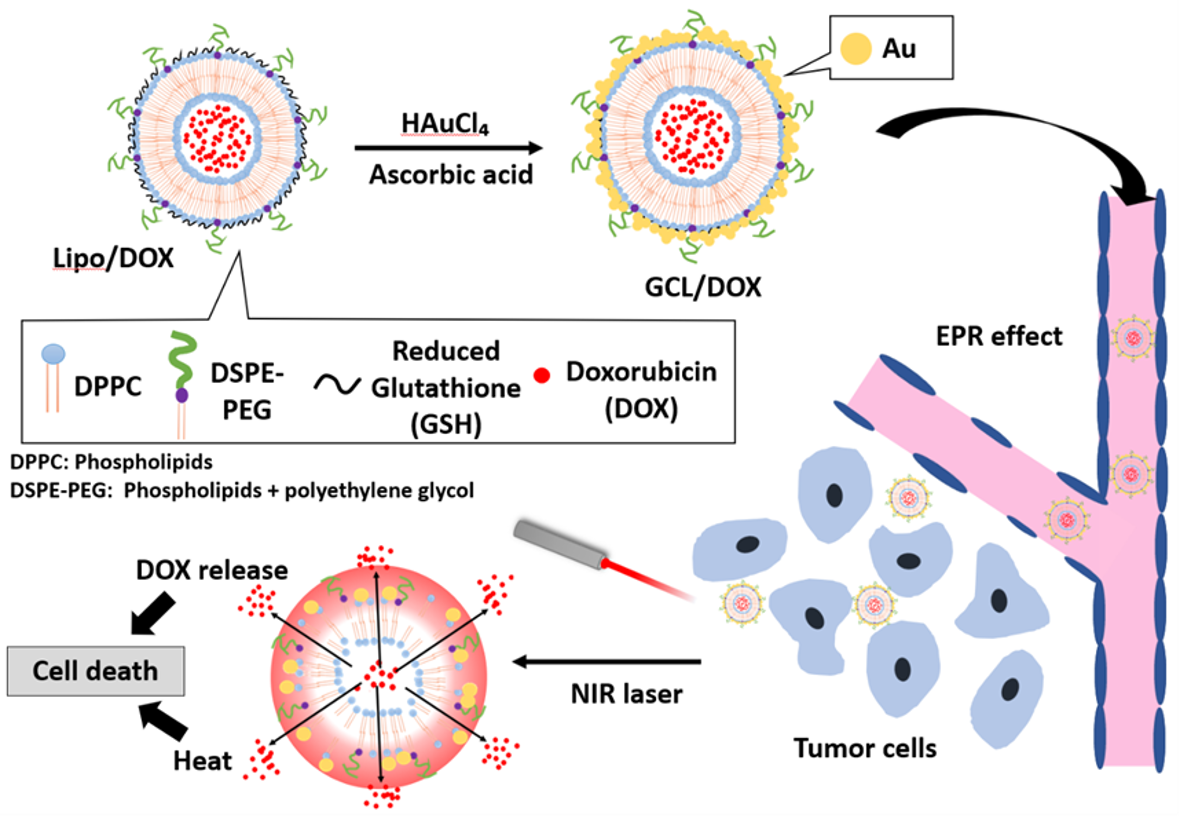
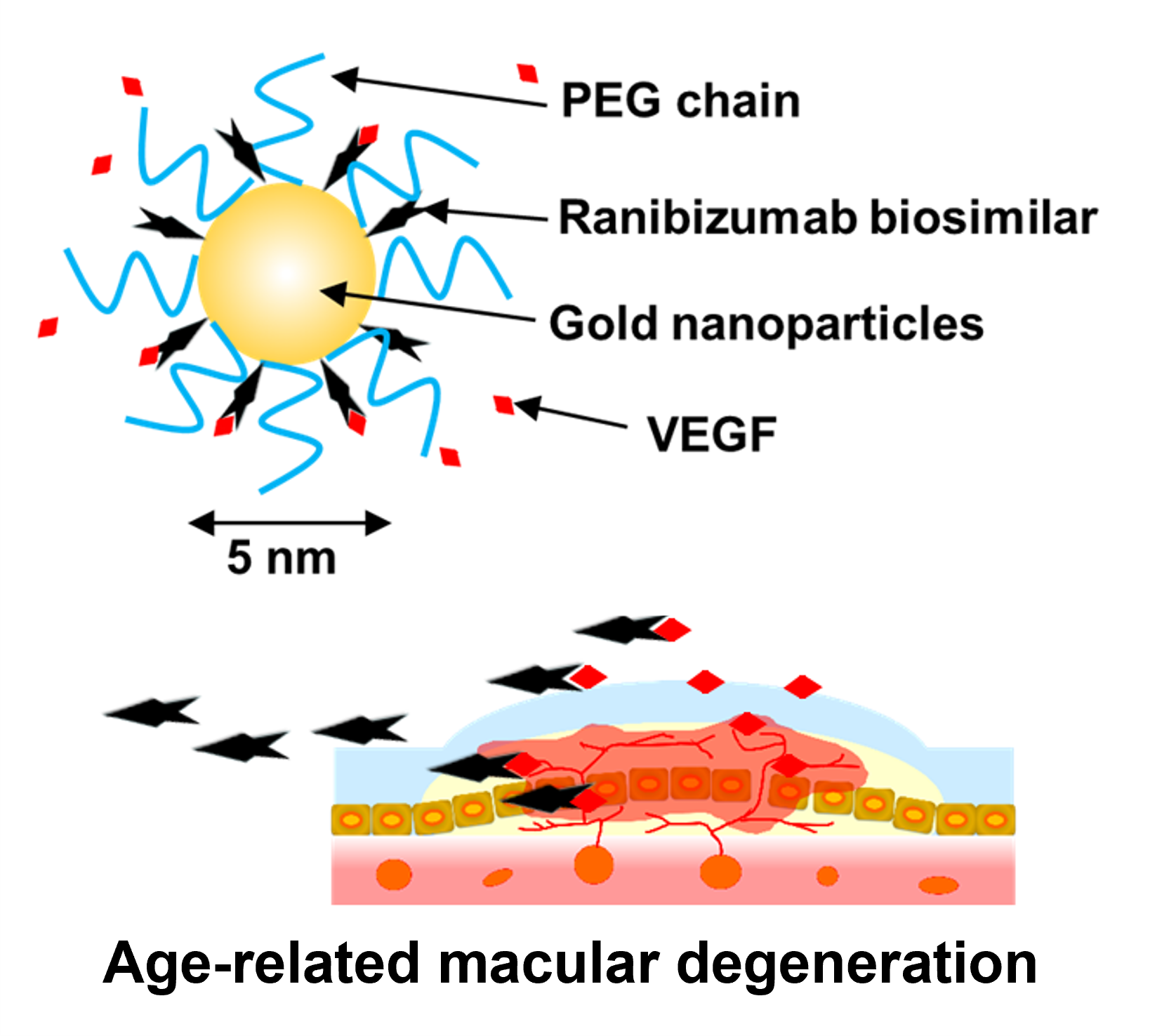
我々は、金ナノ粒子を用いたナノ医薬品のものづくりの研究を行ってきました。金ナノ粒子のアスペクト比を変えることで可視光よりも長波長の光(近赤外線)を吸収することができます。多数の突起を持った金ナノ粒子(金ナノスター)を作製することで近赤外レーザーのエネルギーを効率的に熱変換し、がんの光温熱療法に応用することができることを見出しました(Kondo et al., JDDST 2021)。さらに金ナノスターの表面には、血中滞留性を高めるためのポリマーと光線力学療法に応用可能な光増感剤を結合することで、がんを効率的に治療できる機能性金ナノ粒子を作製しました。また、加齢黄斑変性(眼の新生血管)を抑制するため、金ナノ粒子の表面にanti-VEGF抗体断片を結合したもの、機能性核酸であるsiRNAを表面に結合したもの(Takeuchi et al., JDDST 2017)を作製し、環状オリゴ糖であるシクロデキストリンを結合することで難水溶性薬物を搭載する工夫を行いました(Hashikawa et al., BPB 2018)。また、近赤外レーザーを照射すると、①レーザーのエネルギーを効率的に吸収・発熱しがんに対して光温熱効果をもつだけでなく、同時に粒子に搭載していた光増感剤による光線力学療法としての効果をあわせもつ機能性金属粒子として、突起形状をもつ金ナノ粒子(金ナノスター)に光増感剤とポリエチレングリコールを表面修飾したものを調製しました(Kondo et al., JDDST.2021)